Moderní terapie železem
Akreditované digitalizované sympozium GLOBIFER FORTE v terapii sideropenie a sideropenní anemie
Význam a současné postavení přípravků s hemovým železem u osob s deplecí železa
doc. MUDr. Jiří Slíva, Ph.D.
Ústav farmakologie, 3. LF UK, Praha
Úvod
Aktuálně již několik let probíhá diskuse na téma optimálně vedené perorální suplementace železem v případě jeho deplece. Železo v lidském organismu zastává celou řadu fyziologických úloh a jeho nedostatek se zdaleka neprojevuje pouze jako sideropenická anémie. Neméně významná je totiž i jeho role jako kofaktoru v řadě enzymatických reakcí či v transportu kyslíku na úrovní svalové tkáně, kde je součástí myoglobinu. Zjevná je i kolísající poptávka během našeho života (růst, gravidita, laktace), při vyšší fyzické zátěži nebo u nejrůznějších onemocnění, včetně onkologických. Otázka v těchto případech nezní, zda-li suplementovat, nýbrž jakým způsobem suplementovat. Jistě při těžké depleci je namístě zvolit možnost parenterálního způsobu podání, avšak u většiny nemocných s deficitem železa (nezřídka i při fyziologické hodnotě hemoglobinu – nejdříve klesá feritin, saturace transferinu; anémie je projevem teprve výraznějšího nedostatku!) přistupujeme k perorálnímu způsobu podání. Je-li shoda na vhodnosti perorální aplikace, zbývá již jen volba stran optimálního přípravku.
V zásadě se bavíme o možnosti podání železa ve dvojmocné (Fe2+) nebo trojmocné (Fe3+) formě ve vazbě na organické či anorganické soli; případně ve vazbě na polymerní matrici, ze které je postupně uvolňováno. Nově využívanou možností je podání železa vázaného na molekulu hemu, tedy ve stejné formě, jako se přirozeně nachází v hemoglobinu našich erytrocytů. Nepřekvapí, že se oba zmíněné přístupy (tj. železo nevázané a vázané na hem) vzájemně budou lišit z pohledu svých farmakokinetických vlastností, což se nicméně promítá i do aspektů hodnocené účinnosti a bezpečnosti.
Stručně ke vstřebávání železa
Zcela fyziologicky v běžné stravě přítomná hemová jádra s obsahem dvojmocného železa se ze složitějších struktur (zejm. hemoglobinu či myoglobinu) uvolňují prostou hydrolýzou v žaludku za přispění nízké hodnoty pH a proteolyticky působícího pepsinu, v proximální části tenkého střeva též trypsinu. Uvolněný hem je pak jako celek vstřebáván transportním systémem enterocytů (PCFT/HCP-1). Takto vstřebaný hem může být následně uvolněn do krve avšak současně může být již zde metabolizován za uvolnění železa (2).
Železo, které však není vázáno na strukturu hemu vyžaduje ke své absorpci redukci na dvojmocný stav. To obvykle zajišťuje kyselé žaludeční pH, případně další obsažené kyseliny, včetně např. hojně simultánně podávané kyseliny askorbové. Ke snížení mocnosti železa navíc slouží enzymatická výbava buněk duodena (duodenální cytochrom B) (3). Vlastní absorpce dvojmocného železa pak probíhá prostřednictvím nespecifického transportéru pro dvojmocné kovy DMT-1 (4).
Do enterocytu vstoupivší železo jednou z obou uvedených cest je zde následně vázáno na bílkovinnou složku apoferitin za vzniku feritinu (pozn. agregovaný feritin = hemosiderin) anebo je následně uvolňováno na bazolaterální buněčné straně do krevního oběhu s potenciálem systémového využití. Zde je železo opět oxidováno tak, aby bylo schopno vázat se na transferin. Celý proces vstřebávání železa je precizně regulován v játrech tvořeným hepcidinem (5).
Praktické souvislosti
Hem je biologicky důležitá sloučenina obsahující železo a klíčový zdroj železa v potravě. Historicky se pochybovalo o tom, že by hemové železo mohlo být vstřebáváno enterocytem, a teprve v roce 1955 byla poprvé prokázána absorpce železa získaného z hemu (6). Mnohé studie dokládají, že v západních společnostech tvoří železo získané ze zdrojů hemu, jako je myoglobin a hemoglobin, až dvě třetiny celkových zásob železa průměrného člověka, přestože tvoří pouze jednu třetinu železa, které je skutečně požito. Tato zjevná diskrepance může být vysvětlena lepší vstřebatelností železa vázaného na strukturu hemu (7-9).
Relativní význam dietního hemu lze přičíst jeho vysoké biologické dostupnosti ve srovnání s nehemovým železem v převážně zásaditých podmínkách v tenkém střevě. Kromě toho mnoho složek potravy (zejména třísloviny a fytáty) může na hem nevázané železo chelatovat, které je tak prakticky nevstřebatelné, a tedy zůstává nevyužito (10).
Železo, které není vázáno na hem je tedy mnohem více rizikové z pohledu jeho možné interakce se složkami potravy a navíc i mnohými léky (z důvodu ovlivnění mocenství nebo tvorby obtížně vstřebatelných komplexů). Z pohledu absorpce této formy je třeba zdůraznit i již zmíněný neselektivní transportér pro dvojmocné kovy v duodenu, o nějž musí železo (za předpokladu jeho dvojmocného stavu) soutěžit s mnohými jinými dvojmocnými kationty (10).
Kromě odlišných cest vstřebávání, respektive možnosti užívat danou suplementaci společně se stravou či bez ohledu na případnou další současně užívanou léčbu (pozn.: ani jedno není možné u nehemové formy) představuje při vyšším rozsahu absorpce (11,12) třetí významný benefit železa vázaného v hemu jeho veskrze příznivý bezpečnostní profil. Větší vstřebaný podíl podaného železa je logicky svázán s jeho nižším zůstatkem ve střevě, a je zde tedy nižší riziko pro rozvoj nežádoucích účinků postihujících trávicí trakt.
Při kombinaci železa vázaného v hemovém jádře s nehemovým železem v optimálně zvoleném poměru lze předpokládat využití obou výše popsaných cest absorpce, a tedy i rychlejší úpravu přítomného deficitu. Farmakologickým slovníkem bychom mohli hovořit o komplementaritě obou forem.
Danou skutečnost dokazují proběhlé experimenty i klinická pozorování. V jednom z nich přidání 50 až 85 g masa do jídelníčku vedlo k 1,5 až 4násobnému zvýšení absorpce nehemového železa ve srovnání s bezmasou stravou (13). V roce 2003 byl poprvé ve výživě kojenců studován vliv masa na vstřebávání hemového a nehemového železa. I zde výsledky jasně ukázaly, že přídavek masového prášku u dětí s příkrmem výrazně potencuje absorpci nehemového železa přibližně 2,6násobně – obrázek 1 (14).
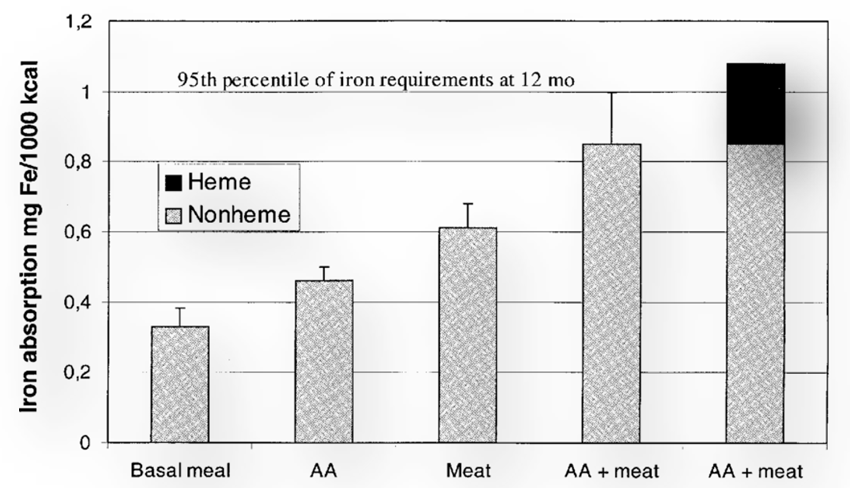
Obrázek 1: Vliv přídavku masa a/nebo kyseliny askorbové (AA) na vstřebaný podíl nehemového a hemového železa (14)
Zkušenosti z České republiky
Možnost cílené perorální suplementace železem vázaným na hem, případně v kombinaci s nehemovým železem je v klinické praxi napříč zeměmi EU využívána již řadu let, a i v České republice máme k dispozici relevantní zkušenosti dokládající přínos pro nemocné.
Již počátkem 90. let minulého století byla zjišťována relativní střevní absorpce hemového a nehemového železa u skupiny žen ve fertilním věku. K běžné stravě jim bylo přidáno 16 mg železa ve formě síranu železnatého a 2 mg železa ve formě hemoglobinu. Jak u žen s fyziologickou výchozí hladinou železa, tak u žen s jeho nedostatkem bylo významně lépe absorbováno hemové železo než síran železnatý: 16,13 ± 8,0 % versus 4,59 ± 3,4 % (p < 0,01) a 22,03 ± 8,9 % versus 9,45 ± 7,8 % (p < 0,05). Autoři studie současně poukazují na velmi dobrou snášenlivost hemové formy železa při zesílení absorpce až o 40 % (15).
Z prostředí ČR zmiňme především zkušenosti autorů se suplementací železem u nemocných s idiopatickým střevním zánětem (IBD), tj. z pohledu rozvoje deplece železa velmi rizikovou skupinou a současně vysoce vnímavou k případným nežádoucím účinkům (16). Pilotní studijní soubor zahrnoval 43 pacienty s IBD ve fázi remise, trpící sideropenií (feritin < 30 μg/l) nebo lehkou sideropenní anémií (Hb 100–120, resp. 130 g/l). Při užívání fixní kombinace hemového a nehemového železa po dobu 12 týdnů autoři zaznamenali statisticky významný nárůst koncentrace hemoglobinu v porovnání s výchozí hodnotou 123,5 g/l v týdnu 0 na 133,5 g/l v týdnu 12 (p = 0,004). Analogicky vzrostl rovněž střední objem erytrocyt, a to z 85,2 fl na 87,3 fl (p = 0,05). Výskyt mírných nežádoucích účinků byl zaznamenán pouze u jediného pacienta (16).
Závěr
Nedostatek železa je v populaci velmi častý, jakkoliv mnohdy může mít klinicky jen málo významné symptomy. Možných příčin je celá řada, od fyziologicky zvýšené poptávky až po nejrůznější patologické procesy. V obou případech je často nezbytné sáhnout po vhodné odpovídající suplementaci. Její různé formy však mají své slabší i silnější stránky vycházející primárně z odlišných mechanismů absorpce. Ty pak de facto určují i rychlost úpravy deficitu či riziko případných doprovodných nežádoucích účinků.
Literatura
1. Khan AA, Quigley JG. Heme and FLVCR-related transporter families SLC48 and SLC49. Mol Aspects Med. 2013 Apr-Jun;34(2-3):669-82.
2. Hooda J, Shah A, Zhang L. Heme, an essential nutrient from dietary proteins, critically impacts diverse physiological and pathological processes. Nutrients. 2014;6(3):1080-1102.
3. McKie AT. The role of Dcytb in iron metabolism: an update. Biochem Soc Trans. 2008 Dec;36(Pt 6):1239-41.
4. Mims MP, Prchal JT. Divalent metal transporter 1. Hematology. 2005 Aug;10(4):339-45.
5. Sangkhae V, Nemeth E. Regulation of the Iron Homeostatic Hormone Hepcidin. Adv Nutr. 2017 Jan 17;8(1):126-136.
6. Walsh RJ, Kaldor I, Brading I, George EP. The availability of iron in meat: some experiments with radioactive iron. Australas Ann Med. 1955 Nov;4(4):272-6.
7. Narasinga BS. Physiology of iron absorption and supplementation. Br Med Bull. 1981;37:25–30.
8. Bezwoda WR, Bothwell TH, Charlton RW et al. The relative dietary importance of haem and non-haem iron. S Afr Med J. 1983;64:552–556.
9. Carpenter CE, Mahoney AW. Contributions of heme and nonheme iron to human nutrition. Crit Rev Food Sci Nutr. 1992;31:333–367.
10. Hallberg L, Solvell L. Absorption of a single dose of iron in man. Acta Med Scand Suppl. 1960;358:19–42.
11. Roughead ZK, Hunt JR. Adaptation in iron absorption: iron supplementation reduces nonheme-iron but not heme-iron absorption from food. Am J Clin Nutr 2000; 72: 982-989.
12. Nam TS, Shim JY, Kim BJ, Rah Y. Clinical Study on the Iron Absorption from Heme-Iron Polypeptide and Nonheme-Iron. Nutritional Sciences 2006; 9: 295-300.
13. Baech SB, Hansen M, Bukhave K, Jensen M, Sørensen SS, Kristensen L, Purslow PP, Skibsted LH, and Sandström B. 2003. Nonheme-iron absorption from a phytate-rich meal is increased by the addition of small amounts of pork meat. Am J Clin Nutr. 77(1):173-9.
14. Hallberg L, Hoppe M, Andersson M, Hulthén L. The role of meat to improve the critical iron balance during weaning. Pediatrics. 2003;111(4 Pt 1):864-70.
15. Ekman M, Reizenstein P. Comparative absorption of ferrous and heme-iron with meals in normal and iron deficient subjects. Z Ernahrungswiss. 1993 Mar;32(1):67-70.
16. Vašátko M, Pešinová V, Malíčková K et al. Hemové železo v substituci sideropenie a sideropenní anémie u pacientů s IBD. Gastroent Hepatol. 2020; 74: 361– 365.